医疗器械不良事件监测与报告制度
为加强医疗器械不良事件监测管理工作,依据国家《医疗器械监督管理条例》、《医疗医械不良事件监测和再评价管理办法(试行)》等规定,制定本制度。
1.医疗器械不良事件是指获准上市的、合格的医疗器械在正常使用情况下发生的导致或可能导致人体伤害的任何与医疗器械预期效果无关的有害事件。伤害事件分一般伤害与严重伤害。严重伤害的含义是指下列情况之一:
(1)危及生命;
(2)导致机体功能的永久性伤害或机体结构永久性损伤;
(3)必须采取医疗措施才能避免的永久性伤害或损伤。
2.不良事件报告及召回的程序
(1)发现可疑的医疗器械不良事件应详细记录,按规定报告。
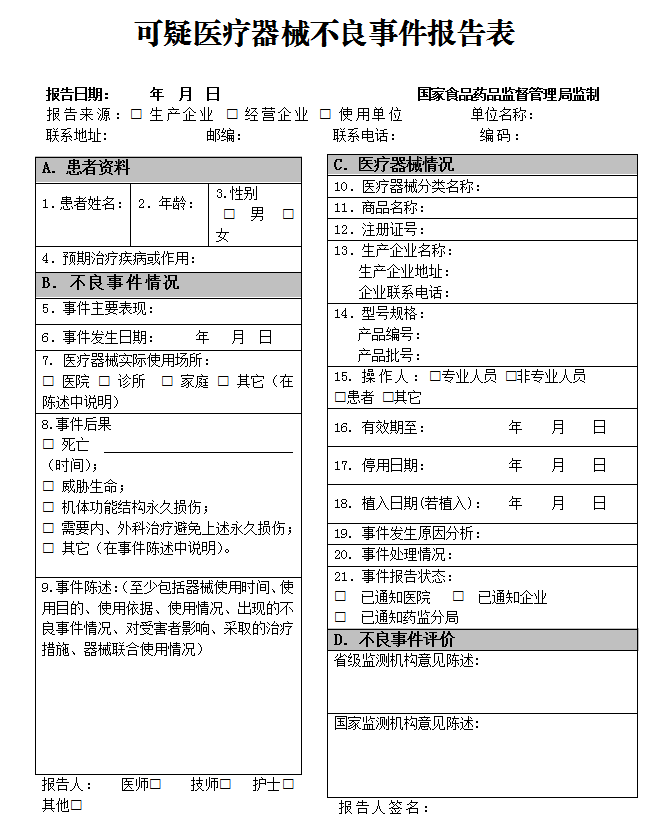
(2)临床使用科室发现或可疑发生医疗器械不良事件,立即填写《可疑医疗器械不良事件报告表》,报设备处。
(3)医疗设备管理委员会在科室上报发生医疗器械不良事件后,对导致死亡的事件于发现或者知悉之日起5个工作日内,导致严重伤害、可能导致严重伤害或死亡的事件于15个工作日内,向上级医疗器械不良事件监测技术机构报告;对突发、群发的医疗器械不良事件,立即向上级医疗器械不良事件监测技术机构报告,并在24小时内报送《可疑医疗器械不良事件报告表》。
(4)在可疑不良事件发生原因未明确前,应主动采取措施,责令使用科室对出现不良事件的医疗器械该批号或该型号的库存产品暂缓放行和停用。
3.不列入医疗器械不良事件的几种情况
在医疗器械使用中,对于可以确定的下列几种情况之一,可以不列入医疗器械不良事件,所产生的病人伤害与死亡应按医疗事故处理程序进行处理。不能明确判定原因的仍按国家可疑医疗器械不良事件处理上报:
(1)超过生产厂商规定的使用期限或重复使用一次性使用器械引起的不良事件;
(2)医疗器械生产厂在技术文件中已标明的可能产生的副作用或有建议性提示的;
(3)使用错误造成的不良事件。不符合生产厂家所规定的操作使用方法,使用者明显运用了厂家明文禁止或建议不能采用的操作行为;
(4)由于病人自身原因、并发症或病人未按医嘱进行的活动造成的不良事件。
4.设备处协助医院主管部门,对本院使用的医疗器械的不良事件信息进行收集、分析、报告和管理,并不断提高临床、医技科室人员防范医疗器械安全风险的意识。
5.医院对隐瞒安全事件的科室,一经查实,根据情节轻重追究责任。
|